Spis treści
-
Początek
-
1 Definicja
-
2 Przyczyny
-
3 Patofizjologia
-
4 Patomorfologia zawału mięśnia sercowego
-
5 Objawy
-
6 Rozpoznanie
-
7 Leczenie
-
8 Powikłania
-
9 Rehabilitacja
-
10 Historia rozpoznania zawału mięśnia sercowego
-
11 Klasyfikacja ICD10
-
12 Zobacz też
-
13 Przypisy
-
14 Bibliografia
-
15 Linki zewnętrzne
Zawał mięśnia sercowego
| Infarctus myocardii | |

| |
| Specjalizacja | |
|---|---|
Zawał mięśnia sercowego, zawał serca, potocznie atak serca (łac. infarctus myocardii) – martwica mięśnia sercowego spowodowana jego niedokrwieniem wskutek zamknięcia tętnicy wieńcowej doprowadzającej krew do serca.
Zawał mięśnia sercowego jest postacią choroby niedokrwiennej serca (obok nagłej śmierci sercowej, dławicy sercowej, przewlekłej choroby niedokrwiennej serca i tak zwanej kardiomiopatii niedokrwiennej). W świecie choroby układu krążenia (w szczególności serca, tętnic i żył) są najczęstszą przyczyną zgonów i mają tendencję wzrastającą[1]. Z powodu schorzeń sercowo-naczyniowych, w tym zawału mięśnia sercowego, umiera dwa razy więcej osób niż z powodu chorób nowotworowych[2].
Zawał mięśnia sercowego pozostaje główną przyczyną zachorowalności i śmiertelności na całym świecie, pomimo poprawy rokowania w ciągu drugiej dekady XXI w. Postęp ten jest wynikiem kilku trendów, w tym poprawy stratyfikacji ryzyka, upowszechnienia stosowania strategii inwazyjnych, wdrożenia systemów opieki zdrowotnej priorytetyzujących natychmiastową rewaskularyzację poprzez przezskórną interwencję wieńcową (lub fibrynolizę), postępu w zakresie leków przeciwpłytkowych i leków przeciwzakrzepowych oraz szerszego stosowania statyn[3].
Definicja
[edytuj | edytuj kod]Zgodnie ze stanowiskiem European Society of Cardiology, American College of Cardiology, American Heart Association i World Health Federation za uniwersalną definicję zawału przyjmuje się obecnie[1][4][5][6]:
- W przypadku świeżego zawału mięśnia serca:
- stwierdzenie podwyższenia stężenia [powyżej 99. centyla zakresu referencyjnego (tzw. wartość odcięcia albo wartość decyzyjna) – wartość zmienna w zależności do producenta testu; przykładowo dla troponiny waha się w granicach 0,01 μg/l do 0,08 μg/l] markerów martwicy mięśnia sercowego, zwłaszcza troponiny (patrz niżej), oraz obecność przynajmniej jednego z objawów:
- typowe objawy niedokrwienia
- świeże zmiany w EKG sugerujące świeży zawał (uniesienie odcinka ST z przeniesieniem chorego do grupy STEMI, świeży blok lewej odnogi pęczka Hisa – LBBB)
- obecność nowych, patologicznych załamków Q w EKG
- stwierdzane w badaniach obrazowych (np. ECHO) nowe odcinkowe zaburzenia kurczliwości ściany serca lub inne wykładniki świeżej martwicy miokardium.
- nagły zgon sercowy z zatrzymaniem akcji serca, do którego doszło przed pobraniem próbki do badania stężenia markerów martwicy mięśnia serca. Objawami sugerującymi przyczynę zawałową są typowe objawy podmiotowe występujące przed zejściem śmiertelnym, zmiany w EKG jak wyżej, stwierdzenie w badaniu sekcyjnym lub koronarograficznym świeżego zakrzepu.
- w przypadku przezskórnej interwencji wieńcowej (PCI) i pierwotnie prawidłowym stężeniu markerów mięśnia serca – stwierdzenie po zabiegu obecności podwyższonego stężenia markerów powyżej 3-krotności 99. centyla zakresu referencyjnego
- w przypadku pomostowania aortalno-wieńcowego (CABG) i pierwotnie prawidłowym stężeniu markerów mięśnia serca – stwierdzenie po zabiegu obecności podwyższonego stężenia markerów powyżej 5-krotności 99. centyla zakresu referencyjnego oraz powstanie świeżych zmian w EKG (LBBB, patologiczne załamki Q), lub zamknięcie przez skrzeplinę nowo wytworzonego pomostu/własnej tętnicy wieńcowej (badania angiograficzne), lub nowe upośledzenie kurczliwości ściany serca w badaniach obrazowych
- stwierdzenie w badaniu sekcyjnym świeżego zawału mięśnia sercowego.
- stwierdzenie podwyższenia stężenia [powyżej 99. centyla zakresu referencyjnego (tzw. wartość odcięcia albo wartość decyzyjna) – wartość zmienna w zależności do producenta testu; przykładowo dla troponiny waha się w granicach 0,01 μg/l do 0,08 μg/l] markerów martwicy mięśnia sercowego, zwłaszcza troponiny (patrz niżej), oraz obecność przynajmniej jednego z objawów:
- W przypadku przebytego zawału mięśnia serca:
- stwierdzenie nowych, patologicznych załamków Q z obecnością lub bez obecności typowych objawów podmiotowych
- stwierdzenie w badaniach obrazowych utraty kurczliwości ściany serca z chwilą gdy najbardziej prawdopodobną przyczyną takich zmian jest niedokrwienie
- stwierdzenie w badaniu sekcyjnym cech przebytego zawału.
Przyczyny
[edytuj | edytuj kod]Do zawału mięśnia sercowego najczęściej dochodzi na tle miażdżycy tętnic wieńcowych w przebiegu choroby wieńcowej (często utożsamianej z chorobą niedokrwienną serca). Może ona doprowadzić do zwężenia tętnicy, pęknięcia blaszki miażdżycowej, zakrzepicy, a ostatecznie do niedrożności tętnicy. Ognisko miażdżycy w ścianie tętnicy wieńcowej nazywane jest właśnie blaszką miażdżycową powstałą na skutek odkładania się cholesterolu LDL (tzw. „zły cholesterol”) i innych tłuszczów w wewnętrznej ścianie tętnicy. Powoduje ona zmniejszenie światła tego naczynia i ograniczenie przepływu krwi – często w tych przypadkach pacjent odczuwa objawy dławicy piersiowej, nazywanej też dusznicą bolesną, przy wysiłku czy zdenerwowaniu[3][7][8][9].
Mechanizmem, który bezpośrednio prowadzi do zawału, jest pęknięcie, z którymi powiązane są kryształki cholesterolu zwiększające ryzyko ich pęknięcia w wyniku urazu mechanicznego i stanu zapalnego[10] lub krwotok do blaszki miażdżycowej. W 90% przypadków bezpośrednią przyczyną zawału mięśnia sercowego jest zakrzep, który powstaje w miejscu pęknięcia blaszki miażdżycowej lub w miejscu zwężonym przez blaszki miażdżycowe. Chorobowe złogi nie tylko zwężają naczynie, ale powodują również spustoszenia w jego ścianie. Gdy w końcu warstwa wewnętrzna pęka, krew wpływa do szczeliny, gromadzą się płytki krwi i uruchomiony zostaje proces krzepnięcia. Tak tworzy się niebezpieczny zakrzep. Jeśli wskutek tych zmian średnica naczynia zostanie zwężona powyżej 2/3 – 3/4 jego średnicy (krytyczne zwężenie tętnicy wieńcowej) wówczas zwykle dokonuje się zawał mięśnia sercowego w obszarze zaopatrywanym przez dane naczynie (mięsień sercowy ulega niedokrwieniu i w ciągu kilku-kilkunastu minut rozpoczyna się jego nieodwracalne uszkodzenie, które w wypadku nieprzywrócenia dopływu krwi prowadzi do powstania ogniska martwicy tego fragmentu mięśnia sercowego)[4][7][8][9].
W rzadkich przypadkach przyczyną zawału może być zator tętnicy wieńcowej (ok. 2,9% zawałów)[9][11]. Jest to skrzeplina krwi, która powstaje w organizmie, a następnie odrywa się i wędruje z prądem krwi. W miejscu jej zatrzymania się może dojść do całkowitego zamknięcia światła naczynia krwionośnego. Z powodów tętniczych ma to jednak miejsce stosunkowo rzadko. Inne rzadkie przyczyny zawału to zmiany zapalne tętnic wieńcowych (np. w kile, chorobie Kawasakiego), uraz (np. w wyniku wypadku komunikacyjnego) lub neuropochodne zaburzenia w regulacji przepływu krwi przez układ naczyń wieńcowych z powodu dysfunkcji mikrokrążenia wieńcowego[9].
Ogniskowa martwica mięśnia sercowego może pojawić się także w przebiegu wstrząsu i przy dużym przeroście mięśnia sercowego. Zawał mięśnia sercowego może być wynikiem ograniczonego ukrwienia serca, które jest narażone na zwiększone zapotrzebowanie na tlen, takie jak gorączka, szybkie tętno, nadczynność tarczycy, niedokrwistość lub niskie ciśnienie krwi. Uszkodzenie lub niepowodzenie procedur, takich jak przezskórna interwencja wieńcowa (PCI) lub pomostowanie aortalno-wieńcowe (CABG), może spowodować zawał mięśnia sercowego. Równie sporadyczną przyczyną zawału jest zamknięcie tętnicy wieńcowej przez nagły skurcz naczynia. Jeśli skurcz ustąpi dostatecznie szybko, chory odczuwa jedynie napad dusznicy. Jest to tak zwana angina Prinzmetala[9][12]. Gdy jednak naczynie pozostanie zamknięte zbyt długo, zaopatrzenie mięśnia sercowego w tlen zostaje upośledzone i rozwija się zawał serca[5][6][8][13].
Czynniki ryzyka
[edytuj | edytuj kod]Zawał mięśnia sercowego występuje na ogół po 40. roku życia, częściej u mężczyzn niż u kobiet, zwłaszcza u osób otyłych i z nadciśnieniem tętniczym. Do czynników ryzyka należą[14]:
- starszy wiek (wiek krytyczny: u mężczyzn 32–50 lat, u kobiet 45-70)
- płeć męska
- palenie tytoniu
- nadciśnienie tętnicze
- inne przyczyny przerostu lewej komory serca (kardiomiopatia, przerost po stosowaniu leków sterydowych)
- wysoki poziom cholesterolu
- zaburzona proporcja pomiędzy cholesterolem LDL i HDL
- obecność patologicznej apolipoproteiny
- wysoki poziom trójglicerydów
- wysoki poziom białka ostrej fazy (białko C-reaktywne, CRP)
- niedobory witamin grupy B, zwłaszcza kwasu foliowego
- wysoki poziom kwasu moczowego
- brak aktywności fizycznej
- osobowość typu A
- marskość wątroby (i wynikające z niej zaburzenia metaboliczne)
- cukrzyca
- predyspozycje rodzinne i genetyczne (zawał w rodzinie w wywiadzie)
- otyłość (zwłaszcza brzuszna).
- choroba Fabry’ego
- przebyty uprzednio zawał mięśnia sercowego.
Patofizjologia
[edytuj | edytuj kod]Większość zawałów serca występuje w wyniku choroby wieńcowej. Są one prawie zawsze spowodowane nagłym zmniejszeniem przepływu krwi w tętnicy wieńcowej, których przyczyną są zmiany miażdżycowe naczyń z dodatkowymi skrzepami krwi („zakrzepica wieńcowa”) i może towarzyszyć im spazmatyczne zwężenie naczyń (skurcz wieńcowy). Obraz kliniczny zależy od lokalizacji, nasilenia i czasu trwania zaburzeń krążenia w mięśniu sercowym. W zawałach mięśnia sercowego z uniesieniem odcinka ST, w ponad 90% przypadków, w ostrym stadium tętnica wieńcowa jest zablokowana przez skrzep krwi (skrzeplinę)[3].
65–75% zawałów mięśnia sercowego z uniesieniem odcinka ST jest wynikiem pęknięcia blaszki miażdżycowej, tj. rozdarcia cienkiej, włóknistej osłonki zapalnej, bogatej w lipidy zmiany w ścianie naczynia[3][4].
Znacznie rzadziej zawał serca jest wynikiem innej choroby. Możliwe są niedrożności tętnic wieńcowych z innych przyczyn, takich jak przedłużające się „skurcze” w dławicy piersiowej Prinzmetala[12] lub w ramach reakcji alergicznej (zespół Kounisa[15]), a także zatory w zapaleniu wsierdzia lub rozsianym wykrzepianiu wewnątrznaczyniowym (DIC). Krwawienie lub guzy w sercu, a także pęknięcia błony wewnętrznej naczynia (intima) wieńcowego w rozwarstwieniu aorty, mogą również prowadzić do niedrożności tętnicy wieńcowej, a tym samym do zawału serca[9]. Komórki w obszarze najgorzej ukrwionym, tuż pod wewnętrzną powierzchnią serca (wsierdzie), są najbardziej podatne na uszkodzenia[16]). Niedokrwienie najpierw dotyka tego obszaru, obszaru podwsierdziowego, a tkanka zaczyna obumierać w ciągu 15–30 minut od utraty dopływu krwi. Martwa tkanka jest otoczona strefą potencjalnie odwracalnego niedokrwienia, która postępuje, przekształcając się w pełnościenny zawał[17]. Początkowa „fala” zawału może wystąpić w ciągu 3–4 godzin[17]. Zmiany te są widoczne w badaniu makroskopowym i nie można ich przewidzieć na podstawie obecności lub braku załamków Q w EKG. Położenie, rozmiar i rozległość zawału zależą od dotkniętej tętnicy, całkowitego zablokowania, czasu trwania zablokowania, obecności naczyń obocznych, zapotrzebowania na tlen i powodzenia procedur interwencyjnych[3].
Mięsień sercowy może zostać uszkodzony także wskutek uszkodzenia reperfuzyjnego. Może ono objawiać się arytmią komorową. Uszkodzenie reperfuzyjne jest konsekwencją wychwytu wapnia i sodu z komórek serca oraz uwolnienia rodników tlenowych podczas reperfuzji. Zjawisko no-reflow – gdy krew nadal nie może dotrzeć do uszkodzonego mięśnia sercowego pomimo usunięcia niedrożności – również przyczynia się do uszkodzenia mięśnia sercowego. Miejscowy obrzęk śródbłonka jest jednym z wielu czynników przyczyniających się do tego zjawiska[9][17][18].
Patomorfologia zawału mięśnia sercowego
[edytuj | edytuj kod]Dokonany zawał mięśnia sercowego pod względem morfologicznym jest zawałem bladym, w którym pojawia się martwica skrzepowa (denaturacyjna). Na obrzeżach ogniska zawałowego mogą powstać ogniska uszkodzenia reperfuzyjnego, w wyniku którego pojedyncze kardiomiocyty ulegają martwicy rozpływnej[19][20].
Przeprowadzony odpowiednio wcześnie zabieg udrożnienia zatkanej tętnicy wieńcowej powoduje, że nie dochodzi do martwicy i kolejnych etapów związanych z obumarciem fragmentu mięśnia sercowego – dlatego tak istotne znaczenie ma leczenie reperfuzyjne.
Makroskopowo zawał jest obszarem bledszej oraz mniej spoistej tkanki niż otaczający mięsień, otoczony wąskimi pasami (rąbkami) barwy czerwonej i żółtej[19][20].
Jeśli zawał pełnościenny jest niepowikłany, typowo przebiega on w czterech okresach[19][20]:

- zawał wczesny (łac. infarctus myocardii recens) w pierwszych kilkunastu godzinach od dokonania martwicy. W tym czasie obszar zawału ujawnia się morfologicznie: pojawia się tzw. rąbek czerwony (pas przekrwienia na obrzeżu ogniska) oraz rąbek żółty (pas granulocytów obojętnochłonnych ulegających stłuszczeniu na obrzeżu ogniska), włókna mięśniowe ulegają fragmentacji i zanika ich poprzeczne prążkowanie
- zawał w stanie rozmiękania (łac. infarctus myocardii in statu emollitionis) trwa od drugiej do dziesiątej – czternastej doby. W tym okresie granulocyty obojętnochłonne i makrofagi uprzątają martwą tkankę, a następnie dochodzi do proliferacji naczyń włosowatych
- zawał w okresie organizacji (łac. infarctus myocardii in statu organisationis) następuje w trzecim i czwartym tygodniu po dokonaniu zawału. Organizacja zawału polega na rozplemie tkanki ziarninowej w miejscu uprzątniętej martwicy
- kształtowanie się blizny pozawałowej (łac. cicatrix post infarctum myocardii) trwa od drugiego do szóstego miesiąca po zawale. Formowanie blizny polega na przekształceniach tkanki ziarninowej, w której przybywa włókien kolagenowych.
Wbrew rozpowszechnionemu poglądowi, nie można w sposób pewny stwierdzić na stole sekcyjnym świeżo dokonanego zawału mięśnia sercowego. Aby potwierdzić zawał serca u zmarłej osoby, osoba taka musi żyć od chwili dokonania zawału co najmniej kilka godzin, aby w jej sercu można było stwierdzić dyskretne cechy martwicy widoczne morfologicznie. Problem wykrywania wczesnych zawałów serca jest ważnym zagadnieniem w medycynie sądowej. Dla stwierdzenia bardzo wczesnych zawałów stosuje się metody immunochemiczne i histochemiczne (np. zwiększenie fuksynofilii uszkodzonych włókien mięśniowych) pozwalające wykazać zmianę aktywności enzymów mięśniowych w ogniskach zawału, ale są to metody mało pewne, zwłaszcza gdy zwłoki zmarłego nie zostały poddane sekcji krótko po zgonie[17].
Objawy
[edytuj | edytuj kod]
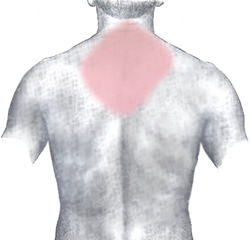
Podmiotowe (subiektywne)
[edytuj | edytuj kod]- bardzo silny ból w klatce piersiowej (może być znacznie osłabiony lub nawet nieobecny u osób chorych na cukrzycę), odczuwany na dużym obszarze klatki piersiowej, trwający ponad 20 minut (dłużej niż w dławicy piersiowej), stale narastający, nieustępujący po odpoczynku i po nitratach (nitrogliceryna), piekący, dławiący, rozpierający, promieniujący do szyi, żuchwy, lewej kończyny górnej, a także na brzuch i plecy.
- panika, lęk przed śmiercią (łac. angor animi)
- duszność zwłaszcza u osób starszych i z rozległym zawałem (duży obszar martwicy)
Przedmiotowe (obiektywne)
[edytuj | edytuj kod]- bladość
- lepki pot (zimne i wilgotne powłoki skórne)
- spadek ciśnienia tętniczego
- tachykardia – wzrost częstości akcji serca, lub inne zaburzenia tętna
- pobudzenie ruchowe
- osłabienie
- mdłości i wymioty
- zawroty głowy lub omdlenie
- sine zabarwienie rąk, stóp, warg
- kołatanie serca (chory czuje, że jego serce mocno bije)
- zmiany osłuchowe w płucach
- temperatura do 38,5 °C
- drętwienie lewej ręki[21]
Czasem zawał prowadzi do nagłej i dramatycznie szybkiej śmierci sercowej, a zgon bywa pierwszym i ostatnim objawem choroby. Do zgonu mogą prowadzić groźne zaburzenia rytmu serca przebiegające ze znacznym przyspieszeniem jego czynności (tachyarytmie komorowe). Około 50% zejść śmiertelnych następuje w ciągu 1–2 godziny od wystąpienia objawów zawału mięśnia sercowego.
W badaniach dodatkowych
[edytuj | edytuj kod]Obserwuje się zmiany w[22]:
- obecność markerów zawału we krwi (badanie decyzyjne przy rozpoznawaniu zawału)
- zmiany elektrokardiograficzne
- podwyższony poziom glukozy we krwi
- przyspieszone opadanie krwinek (OB)
- wzrost liczby leukocytów we krwi obwodowej (zwiększona leukocytoza)
Podział kliniczny zawału (ostre zespoły wieńcowe)
[edytuj | edytuj kod]Z punktu widzenia praktycznego, obecnie ostre niedokrwienie mięśnia sercowego nazywa się ostrym zespołem wieńcowym (OZW) (ang. ACS – Acute Coronary Syndromes) i dzieli się na następujące jednostki kliniczne, gdyż implikuje to sposób postępowania leczniczego[1][8]:
- niestabilna choroba wieńcowa (ang. UA – Unstable Angina)
- zawał mięśnia sercowego
- bez uniesienia odcinka ST elektrokardiogramu (ang. NSTEMI – Non ST-elevation Myocardial Infarction)
- z uniesieniem odcinka ST elektrokardiogramu – (ang. STEMI – ST-Elevation Myocardial Infarction)
- nagły zgon sercowy.
Niestabilną chorobą wieńcową (UA) oraz zawał serca bez uniesienia ST (NSTEMI) zalicza się jednej grupy, gdyż oba te stany chorobowe powstają z podobnej przyczyny – pęknięcia blaszki miażdżycowej z następowym narastaniem zakrzepu płytkowego, co doprowadza do zwężenia, ale nie do całkowitego zamknięcia światła naczynia[8].
W przypadku całkowitego zamknięcia naczynia dochodzi do zawału mięśnia sercowego z uniesieniem odcinka ST (STEMI) lub bardziej morfologicznie rzecz ujmując – zawału pełnościennego lub w szczególnie dramatycznych wypadkach – nagłego zgonu sercowego[1].
Istnieje również bardziej precyzyjny system klasyfikacji, oparty na międzynarodowym konsensusie z 2012 roku. Klasyfikuje ona zawały mięśnia sercowego na pięć typów[6]:
- Typ I – samoistny zawał serca związany z erozją i/lub pęknięciem blaszki miażdżycowej, szczelinowaniem lub rozwarstwieniem
- Typ II – zawał serca związany z niedokrwieniem, np. ze zwiększonym zapotrzebowaniem na tlen lub zmniejszoną podażą, np. skurczem tętnicy wieńcowej, zatorem wieńcowym, anemią, arytmią, nadciśnieniem tętniczym lub niedociśnieniem tętniczym
- Typ III – niespodziewany zgon sercowy, w tym zatrzymanie krążenia, w którym objawy mogą sugerować zawał serca, EKG może zostać wykonane z sugestywnymi zmianami lub skrzep krwi w tętnicy wieńcowej zostanie wykryty za pomocą angiografii i/lub autopsji, ale zgon nastąpił przed pobraniem próbek krwi, przed wzrostem stężenia biomarkera sercowego lub, w rzadkich przypadkach, bez pobrania biomarkerów sercowych
- Typ IVa – związany z przezskórną interwencją wieńcową (PCI)
- Typ IVb – związany z zakrzepicą stentu udokumentowaną angiografią lub autopsją
- Typ V – związany z pomostowaniem aortalno-wieńcowym (CABG)
Kody Międzynarodowej Statystycznej Klasyfikacji Chorób i Problemów Zdrowotnych ICD-10 dotyczące zawału serca:
- (I21) Ostry zawał serca
- (I22) Ponowny zawał serca („dorzut”)
- (I23) Powikłania występujące w czasie ostrego zawału serca (krwiak osierdzia, ubytek przegrody międzyprzedsionkowej lub międzykomorowej, pęknięcie ściany serca, strun ścięgnistych, mięśnia brodawkowatego, skrzeplina przedsionka, uszka przedsionka i komory).
Rozpoznanie
[edytuj | edytuj kod]Zawał serca można rozpoznać na podstawie przekroczenia norm stężeń biochemicznych markerów uszkodzenia mięśnia sercowego we krwi i zmian w zapisie EKG[22][23].
Enzymy wskaźnikowe w zawale serca
[edytuj | edytuj kod]
Diagnostyka biochemiczna zawału mięśnia sercowego opiera się na oznaczaniu w surowicy krwi enzymów i innych białek uwalnianych do krwi w wyniku martwicy kardiomiocytów. W zależności od metod oznaczania tych białek, wartości referencyjne i wartości odcięcia mogą się znacznie różnić pomiędzy poszczególnymi ośrodkami[23].
Markery diagnostyczne
[edytuj | edytuj kod]- cTnT i cTnI (izoformy troponin najbardziej swoiste dla mięśnia sercowego) – stężenie podnosi się od 3. godziny po zawale, osiągając szczyt po ok. 24 godz. normalizuje się pomiędzy 6. a 10. dniem i ma wiodące znaczenie w rozpoznaniu zawału serca[22][23][24],
- CPK lub CK (kinaza kreatynowa) – poziom wzrasta 2–5 godzin po zawale, szczyt osiąga 24 godziny po zawale, a normalizuje się w 2.-3. dobie[23][25]
- CK-MB – frakcja CPK z dimerami M i B, specyficzna dla mięśnia sercowego[23],
- Fosforylaza glikogenu GPBB pojawia się po 1–2 godzinach po wystąpieniu bólu w klatce piersiowej, a to sprawia, że jest szybką metodą rozpoznania zawału serca w jego wczesnej fazie; szczyt osiąga po 6 godzinach[26],
- Sercowe białko wiążące kwasy tłuszczowe, czyli h-FABP (ang. heart-fatty acids binding protein) – pojawia się w osoczu po 30–210 minut od wystąpienia objawów, szczyt stężenia osiąga po ok. 6 godzinach, natomiast po 24 godzinach powraca do wartości wyjściowych[26],
- Mioglobina pojawia się 2–4 godziny od początku objawów, osiąga szczyt po 6–7 godzinach i powraca do wartości wyjściowych po 18–24 godzinach[22].
Badania krwi są powtarzane w określonych odstępach czasu (co 4–8 godzin), aby monitorować zmiany w poziomie markerów sercowych, co pomaga w ocenie rozległości uszkodzenia mięśnia sercowego oraz czasu wystąpienia zawału[23].
W użyciu są szybkie testy do stosowania przez ratowników medycznych już w okresie przedszpitalnym, które wykrywają w ciągu 6–7 minut podwyższone enzymy, świadczące o wystąpieniu zawału mięśnia sercowego[27].
W praktyce klinicznej określa się zazwyczaj
[edytuj | edytuj kod]Najczęściej bada się[22]:
- jedną z frakcji troponin swoistych dla mięśnia sercowego, które są wiodące w diagnozowaniu
- CKMB
- morfologię + podstawowe parametry układu krzepnięcia
- OB
Wraz z dwukrotnym zapisem EKG (w krótkim odstępie czasu) dla doświadczonego zespołu pozwala to prawie natychmiast, jednoznacznie i bez ryzyka pomyłki potwierdzić lub wykluczyć rozpoznanie[1].
W niektórych ośrodkach bada się nadal jeszcze inne wskaźniki, ale część tych markerów nie jest specyficzna dla zawału, np.: podniesienie poziomu ALAT, ASPAT, GGTP czy LDH towarzyszy także innym schorzeniom, np. wątroby, czy podczas hemolizy. Ich podwyższony poziom nie musi świadczyć o zawale[22][28].
Zapis EKG
[edytuj | edytuj kod]Ewolucja zmian w zapisie ekg może trwać od kilku godzin do kilku dni[22]:


(patologiczny załamek Q)

(uniesiony odcinek ST)

(ujemny załamek T)
Najwcześniej do normy dochodzi fala Pardeego. Załamek T normalizuje się w ciągu kilku miesięcy, a dziura elektryczna może pozostać na stałe w zapisie EKG jako ślad po przebytym zawale.
W zapisie EKG różnicować można kolejne warstwy ogniska zawałowego w ścianie mięśnia sercowego (od „wewnątrz”):
- strefa martwicy – patologiczny załamek Q (dłuższy niż 0,04 s oraz wyższy niż 25% załamka R)
- strefa uszkodzenia – fala Pardeego, uniesiony odcinek ST
- strefa niedotlenienia – ujemny załamek T.
Powyższe 3 strefy i ich obraz w EKG są charakterystycznymi cechami zawału serca w elektrokardiografii. W zależności od lokalizacji zawału poszukujemy ich w różnych odprowadzeniach, a na tej podstawie wysuwamy wnioski na temat lokalizacji zawału:
- zawał rozległy przedni (łac. infarctus myocardii parietis anterioris externus) – odprowadzenia V1-V6, I, aVL
- zawał przednio-przegrodowy (łac. infarctus myocardii anteroseptalis) – odprowadzenia V1, V2, V3, V4
- zawał przedniej ściany serca (łac. infarctus myocardii parietis anterioris) – odprowadzenia V3, V4
- zawał przednio-boczny (łac. infarctus myocardii anterolateralis) – odprowadzenia V3-V6, I, aVL
- zawał dolnej ściany serca (łac. infarctus myocardii parietis inferioris) – odprowadzenia II, III, aVF
- zawał tylnej ściany serca (łac. infarctus myocardii parietis posterioris) – odprowadzenia V1, V2 (UWAGA! „Efekt lustra”, tzn. załamek T dodatni, zamiast ujemnego czy wysoki załamek R zamiast patologicznego załamka Q).
Diagnostyka obrazowa
[edytuj | edytuj kod]Diagnostyka obrazowa, w tym echokardiografia, koronarografia, tomografia komputerowa (CT) oraz rezonans magnetyczny (MRI), pozwala na ocenę funkcji skurczowej lewej komory, identyfikację obszarów niedokrwienia oraz ocenę stanu tętnic wieńcowych, co jest niezbędne do planowania leczenia reperfuzyjnego[23].
Różnicowanie bólu wieńcowego z bólem zawałowym
[edytuj | edytuj kod]| Cecha | Ból wieńcowy | Ból zawałowy |
|---|---|---|
| Charakter: | gniotący/piekący ból zamostkowy, penetrujący do lewej ręki, przestrzeni międzyłopatkowej, żuchwy | |
| Czas trwania: | 5-17 min | >30 min |
| Wpływ nitratów: | Ustaje po nitratach | Nie ustaje po nitratach |
| Wpływ wysiłku: | występuje dopiero po wysiłku | występuje nawet podczas spoczynku |
Leczenie
[edytuj | edytuj kod]Pierwsza pomoc przy zawale
[edytuj | edytuj kod]Pierwsza pomoc sprowadza się do ułożenia chorego w pozycji półsiedzącej (o ile jest przytomny) lub bocznej ustalonej (jeśli jest nieprzytomny), wezwaniu fachowej pomocy medycznej i kontroli tętna i oddechu (jeśli ustanie praca serca i oddech należy rozpocząć resuscytację krążeniowo-oddechową). W etapie przedszpitalnym/medyczno ratunkowym stosuje się tzw. schemat OH BATON (Opioid – Morfina, Heparyna niefrakcjonowana, Beta-adrenolityk, Aspiryna, Tikagrelor, O-tlen, Nitrogliceryna). Pacjentowi podaje się mieszaninę tlenu z powietrzem maską twarzową, nitroglicerynę 0,4–0,8 mg podjęzykowo; aspiryna 300–500 mg doustnie; dożylna analgezja (Morfina); metoprolol p.o./i.v.; infuzja dożylna nitrogliceryny (jeśli ciśnienie pozwala) z infuzją 0,9% NaCl. Także jest ważne stworzyć kardiomonitoring – w ciągu transportu pacjent musi być monitorowany, aby w odpowiedniej chwili diagnozować zaburzenia rytmu serca[1][4][8][29][30] i natychmiast wezwać karetkę.
Nie podawać nitrogliceryny przy objawach wstrząsu: pacjent blady, zlany zimnym potem z niskim ciśnieniem tętniczym. Nie wolno podawać preparatów zawierających diklofenak, odradza się podawanie glikozydów nasercowych czy jakichkolwiek innych leków (w tym nasercowych lub nadciśnieniowych). Czas od wystąpienia pierwszych objawów do momentu dostarczenia chorego do szpitala decyduje o możliwości wykonania mechanicznej reperfuzji naczynia lub podania leków trombolitycznych, co ma decydujące znaczenie dla przeżywalności i stopnia uszkodzenia mięśnia sercowego[1][7].
Ostry zawał serca jest stanem naglącym, wymagającym szybkiej interwencji medycznej[1]. Jednak około 60% chorych umierających z powodu zawału, ginie w pierwszej godzinie choroby – najczęściej jeszcze przed uzyskaniem kwalifikowanej pomocy lekarskiej. Jeśli ból w klatce piersiowej utrzymuje się około 15 minut, nie należy zwlekać z wezwaniem pomocy. Pierwsza godzina ataku serca jest rozstrzygająca, jednak w praktyce sprowadza się to do pierwszych 4 godzin. Opóźnienie leczenia wynika najczęściej z winy niezdecydowanego pacjenta (ociąganie się z wezwaniem pomocy lekarskiej dotyczy 62% pacjentów). Opóźnienie z winy transportu związane jest z niepotrzebnym skierowaniem chorego z zawałem do ośrodka bez możliwości przeprowadzenia zabiegu PCI i ponownego transportu do szpitala z pracownią hemodynamiczną. Z tego powodu wypracowano tzw. system transportu bezpośredniego, w ramach którego chory z podejrzeniem zawału serca jest transportowany bezpośrednio z domu, czy gabinetu lekarza pierwszego kontaktu, do pracowni hemodynamiki[7].
W niektórych krajach (ostatnio także w Polsce) propaguje się dostęp przeszkolonych osób do defibrylatorów, w celu leczenia nagłego zatrzymania krążenia u osób z zawałem mięśnia sercowego.
Lekarz, jeżeli istnieje podejrzenie zawału, dokonuje pomiarów tętna, ciśnienia krwi oraz podłącza chorego do stałego monitoringu. Wykonuje EKG oraz zapewnia stały dostęp do żyły poprzez założenie kaniuli lub w cięższych przypadkach wkłucia centralnego. W przypadku gdy jest to wymagane, podaje tlen, który powinien być nawilżony. Powinien pobrać krew do badań oraz walczyć z bólem[1].
Podczas zawału serca nie można dopuścić do stworzenia się zakrzepów, dlatego podaje się na samym początku kwas acetylosalicylowy (aspiryna) w dawce co najmniej 300 mg (aktualnie podanie aspiryny traktowane jest jako rutynowe postępowanie przedszpitalne), obecnie zaleca się również rutynowe podawanie klopidogrelu w dawce 300 mg lub 600 mg u tych pacjentów, u których planujemy PCI oraz heparynę w dawce 40-70 j.m./kg. Płytki krwi. W każdym przypadku podejrzenia zawału (potwierdzonego lub nie) pacjenta należy pilnie i jak najszybciej dostarczyć do specjalistycznego ośrodka z dyżurną pracownią hemodynamiczną lub oddziałem kardiochirurgii interwencyjnej[1].
Zawał prawej komory
[edytuj | edytuj kod]Zawał obejmujący swoim zasięgiem mięsień prawej komory serca, mimo że nie częsty, jest przypadkiem szczególnym, w którym postępowanie różni się od procedur przyjętych w zawale lewokomorowym. Zawał prawej komory najczęściej przebiega z podwyższonym ciśnieniem w żyłach szyjnych‚ bradykardią i blokiem przedsionkowo-komorowym, ze względu na towarzyszące uszkodzenie węzła przedsionkowo-komorowego, zaopatrywanego w krew przez prawą tętnicę wieńcową. Za tym rozpoznaniem przemawia uniesienie ST w V4R; EKG z tego odprowadzenia powinno zostać zarejestrowane u każdego chorego z zawałem ściany dolnej lub we wstrząsie. Bardzo charakterystyczne są także załamki Q i uniesienie odcinka ST w V1 – V3. W ostrej fazie zawału nie wolno stosować azotanów (nitrogliceryna), ACEI oraz diuretyków. Należy zwalczać hipotonię wlewem płynów infuzyjnych, początkowo szybko, z kontrolą parametrów hemodynamicznych oraz podawaniem leków o działaniu inotropowym dodatnim. W przypadku znacznie nasilonej bradykardii, gdy jest to możliwe, należy zastosować czasową stymulację serca celem uzyskania poprawy hemodynamicznej. Zwiększenie powrotu żylnego do prawej komory można uzyskać układając chorego w pozycji Trendelenburga[22].
Postępowanie medyczne przy ostrym zawale serca
[edytuj | edytuj kod]Udrożnienie zamkniętego naczynia wieńcowego
[edytuj | edytuj kod]Obecnie stosuje się trzy metody udrożnienia naczyń wieńcowych w zawale:
Zabieg angioplastyki wieńcowej
[edytuj | edytuj kod]Najnowsze badania wskazują, że najbardziej skuteczną metodą leczenia zawału jest przezskórna interwencja wieńcowa (PCI)[1][4]. Wykazano, że pierwotna angioplastyka skuteczniej niż tromboliza chroni mięsień sercowy przed skutkami niedokrwienia oraz skuteczniej przywraca prawidłową anatomię tętnicy dozawałowej, minimalizując rezydualne zwężenie. Udrożnienie tętnicy dozawałowej uzyskano u 95% chorych leczonych PCI i u 80% pacjentów, u których zastosowano trombolizę[31].
Kluczowym dla powodzenia zabiegu jest czas, jaki mija od pierwszych objawów do chwili, gdy pacjent trafia do szpitala na zabieg. W języku angielskim czas ten określa się jako door-to-balloon – od drzwi (chorego) do balonika[32].
Przed zabiegiem PCI (lub najpóźniej w momencie zabiegu) zaleca się przyjmowanie silnego inhibitora P2Y12 (prasugrelu lub tikagreloru) albo klopidogrelu i przez 12 miesięcy po zabiegu, chyba że występują przeciwwskazania, takie jak nadmierne ryzyko krwawienia[1].
Zabieg angioplastyki wieńcowej wykonuje się w pracowniach hemodynamiki oddziałów kardiologii lub kardiologii inwazyjnej, najlepiej w dyżurujących 24 godziny w siedem dni w tygodniu. Polega on na uwidocznieniu i udrożnieniu tętnicy dozawałowej[31].
Poprzez nakłucie w tętnicy udowej lub promieniowej wprowadza się do układu tętniczego specjalne cewniki skonstruowane przez Melvina Judkinsa, które po umieszczeniu w opuszce aorty pozwalają zobrazować tętnice wieńcowe serca. Wyróżnia się cewniki lewe i prawe, gdzie za pomocą lewego cewnika można podejrzeć lewą tętnice wieńcową składającą się z dwóch głównych gałęzi tj. gałęzi przedniej zstępującej (międzykomorowej przedniej) oraz gałęzi okalającej, a za pomocą prawego cewnika prawą tętnice wieńcową. Cały proces wprowadzania cewnika monitorowany jest na monitorze RTG. Następnie do tętnic poprzez cewniki wprowadza się płyn kontrastujący (koronarografia), który umożliwia zaobserwowanie ich przebiegu i zmian chorobowych. W miejsce zwężenia lub zakrzepicy zawałowej wprowadza się cieniutki drucik zwany prowadnikiem wieńcowym, który przechodzi przez zmianę (zwężenie) w tętnicy. Po prowadniku wieńcowym wprowadza się w miejsce zwężenia cewnik zaopatrzony w balonik do którego pompuje się płyn (jest to najczęściej mieszanka kontrastu z solą fizjologiczną) pod ciśnieniem od kilku do kilkunastu atmosfer. Balonik rozszerza światło zwężonego (zamkniętego) naczynia wieńcowego normalizując w nim przepływ krwi. Poszerzenia światła naczynia za pomocą balona (bez użycia stentu) nazywa się dylatacją, natomiast gdy na cewniku z balonem znajduje się stent (jest to metalowa siateczka, która stabilizuje rozszerzone naczynie) nazywamy dylatacja z wszczepieniem stentu. To najskuteczniejsza metoda leczenia świeżego zawału serca z uniesieniem odcinka ST. Czasami może się zdarzyć, że zabieg angioplastyki jest niemożliwy do wykonania i wtedy konieczna jest operacja pomostowania aortalno-wieńcowego (bypass), która wiąże się z koniecznością wykonania torakotomii. Wykonanie koronarografii, która poprzedza angioplastykę, daje możliwość dokładnej oceny tętnic wieńcowych i umożliwia wybór optymalnego sposobu rewaskularyzacji (pierwotna angioplastyka PCI vs. pomostowanie aortalno-wieńcowe), pozwala także na ocenę ryzyka na podstawie nasilenia zmian w tętnicach wieńcowych[1][31][33].
Optymalną metodą leczenia świeżego zawału serca (do 12 godz. od początku bólu) jest przezskórna interwencja wieńcowa[34], pod warunkiem że jest wykonywana w ośrodku pełniącym przez siedem dni w tygodniu 24-godzinny dyżur zawałowy przez doświadczonych operatorów w ciągu 90 minut od pierwszego kontaktu z lekarzem (pierwotna angioplastyka wieńcowa). W każdym przypadku, gdy nie są znane istotne przeciwwskazania, należy rozważyć i zaproponować choremu właśnie taką metodę postępowania. Zdiagnozowanie zawału pełnościennego serca przez personel ratowniczy przed przyjęciem do szpitala umożliwia wcześniejsze zawiadomienie pracowni hemodynamiki, co skutkuje wcześniejszym zabiegiem angioplastyki wieńcowej[1][4][22].
Lekarze na oddziałach ratunkowych powinni być zaopatrzeni w specjalne formularze, które opisują algorytm postępowania, kończący się (przy potwierdzeniu zawału) skierowaniem pacjenta na leczenie trombolityczne lub do zabiegu angioplastyki. Inne postępowanie jest błędem w sztuce lekarskiej[1].
W celu umożliwienia jak najszybszego dostępu do angioplastyki wszystkim pacjentom z ostrym zawałem serca na Mazowszu zespół pracowni hemodynamiki Narodowego Instytutu Kardiologii wprowadził możliwość przywiezienia pacjenta przez zespół karetki reanimacyjnej pogotowia ratunkowego bezpośrednio z miejsca zachorowania (np. z domu pacjenta), po teletransmisji EKG, do pracowni hemodynamiki bez konieczności potwierdzania rozpoznania zawału serca w szpitalu powiatowym zlokalizowanym najbliżej miejsca zachorowania (system transportu bezpośredniego)[7][35].
Tak prowadzony pacjent, jeśli trafił do lekarza w odpowiednim czasie, ma szanse na pełne wyleczenie – to znaczy uniknięcie martwicy fragmentu mięśnia sercowego i jakichkolwiek powikłań z tym związanych w przyszłości. Możliwy jest w takiej sytuacji pełny powrót do zdrowia i aktywności zawodowej[7].
Podanie leków fibrolitycznych
[edytuj | edytuj kod]Jeśli PCI nie można wykonać w ciągu 90 do 120 minut od wystąpienia objawów w przypadku STEMI, zaleca się fibrynolizę, najlepiej w ciągu 30 minut od przybycia do szpitala. Fibrynoliza nie jest zalecana w sytuacjach, gdy wiąże się z wysokim ryzykiem krwawienia, po przebytym udarze niedokrwiennym lub krwawieniu do mózgu lub w przypadku ciężkiego nadciśnienia tętniczego[4][3].
Leczenie zachowawcze i obserwacja chorego, czyli odstąpienie od udrożnienia zablokowanego naczynia wieńcowego przy świeżym zawale (za pomocą angioplastyki lub leków trombolitycznych) wobec obecnej wiedzy medycznej należy uznać za poważny błąd w sztuce lekarskiej, istotnie zagrażający życiu pacjenta i powodujący w przyszłości dużą szansę na to, iż chory zostanie inwalidą[1].
Jeśli ośrodek nie ma możliwości wykonania angioplastyki lub podania leków trombolitycznych to pacjent ze świeżym zawałem nie powinien do takiego ośrodka trafić. Małe, lokalne szpitale, bez pracowni kardiologii inwazyjnej i pracowni hemodynamiki, nie powinny przyjmować pacjentów ze świeżym zawałem serca, lecz kierować ich do ośrodków specjalistycznych[1].
Fibrynoliza jest ważną strategią reperfuzji w sytuacjach, gdy pierwotna PCI nie może zostać zastosowana w odpowiednim czasie. Po rozpoczęciu leczenia litycznego zaleca się transport pacjentów do szpitala wykonującego PCI. W przypadku nieskuteczności fibrynolizy lub jeśli istnieją dowody na reokluzję lub ponowny zawał z nawrotem uniesienia odcinka ST, konieczne jest natychmiastowe wykonanie angiografii i ratunkowego PCI. Odradza się ponowną fibrynolizę. Nawet jeśli fibrynoliza prawdopodobnie zakończy się sukcesem, zaleca się rutynową wczesną angiografię (2–24 godziny po fibrynolizie), o ile nie ma przeciwwskazań[1].
Postępowanie w późnym zawale, gdy pacjent trafił na oddział po więcej niż 12 godzinach od początku bólu nie jest jednoznaczne. Zakłada się jednak, że wykonanie angioplastyki w takim przypadku należy odłożyć do powstania blizny, lecz docelowo zabieg udrożnienia wykonać. Na razie istnieje zbyt mało dowodów naukowych, które mogłyby jednoznacznie określić postępowanie w takich przypadkach[31].
Pomostowanie aortalno-wieńcowe
[edytuj | edytuj kod]W wybranych przypadkach, gdy niemożliwe jest zastosowanie leków trombolitycznych lub wykonania pierwotnej angioplastyki wieńcowej (głównie w przypadkach zaawansowanych zmian miażdżycowych w wielu odcinkach kilku tętnic równocześnie) stosuje się zabieg operacyjny mający na celu wykonanie pomostów aortalno-wieńcowych (nazwa potoczna: by-passów), poprawiających ukrwienie serca. Operacja wiąże się uzyskaniem dostępu do narządów klatki piersiowej poprzez torakotomię (otwarcie klatki piersiowej) na oddziałach kardiochirurgii[1][33].
Leczenie przeciwbólowe
[edytuj | edytuj kod]Pierwszym lekiem przeciwbólowym podawanym pacjentowi jest morfina, podawana dożylnie. Początkowo 5 mg w ciągu 2 min, a następnie 2 mg co 5-15 min. Maksymalna dawka wynosi 30 mg. Jednocześnie z opioidem można podać lek przeciwwymiotny, np. Metoklopramid 5–10 mg dożylnie[22].
Leczenie pozawałowe
[edytuj | edytuj kod]Objęcie pacjentów ze świeżym zawałem serca intensywną opieką kardiologiczną istotnie zmniejsza śmiertelność szpitalną i pozaszpitlaną chorych, stwarzając większą szansę przeżycia. Wśród najczęściej stosowanych leków wymienia się: leki beta-adrenolityczne (beta-blokery), które zmniejszają zapotrzebowanie mięśnia sercowego na tlen przez wpływ na częstotliwość rytmu i kurczliwości serca, antagonisty kanału wapniowego, które powodują rozkurcz naczyń wieńcowych, zmniejszenie kurczliwości serca, a w następstwie zmniejszenie zapotrzebowania na tlen oraz inhibitory konwertazy angiotensyny (ACEI, zofenopryl), które utrzymują ciśnienie krwi na odpowiednim poziomie, umożliwiając swobodny przepływ w organizmie bogatej w substancje odżywcze, natlenowanej krwi, nie obciążając jednocześnie układu sercowo-naczyniowego. Ich działanie polega na zapobieganiu przekształcenia angiotensyny I na angiotensynę II, powodującą zwężanie naczyń krwionośnych. Gdy naczynia krwionośne nie są nadmiernie zwężone, krew płynie swobodniej, nie obciążając dodatkowo serca. Wnioski z przeprowadzonych badań klinicznych wskazują, że zastosowanie ACEI w ciągu pierwszych 24 godzin po zawale mięśnia sercowego zwiększa szanse na przeżycie[36]. Korzyści w zastosowaniu takiej terapii zależą jednak od wyboru leku. Zofenopryl jest silniej powiązany z sercową ACE i mniej zależny od bradykininy, co zwiększa siłę pierwotnej kardioprotekcji przez redukcję ryzyka ciężkiego nadciśnienia tętniczego. W związku z tym wczesne podanie ACEI u chorych po zawale mięśnia sercowego jest skuteczne, ale powinno opierać się na wyborze najbardziej odpowiedniego leku, którym jako lek pierwszego rzutu wskazywany jest zofenopryl[37].
Leczenie powikłań
[edytuj | edytuj kod]Następstwa ataku serca są zróżnicowane w zależności od rozległości uszkodzenia mięśnia sercowego. Ognisko zawałowe wielkości około 10% masy mięśnia komory nie powoduje trwałego inwalidztwa (możliwy jest powrót chorego do normalnego funkcjonowania). Bardziej rozległy obszar martwicy (25%) upośledza funkcje serca jako pompy, prowadząc do jego niewydolności. Martwica obejmująca 40% mięśnia sercowego i więcej może wywołać wstrząs kardiogenny, co również może stanowić przyczynę nagłego zgonu. Przebieg kliniczny choroby zależy też od lokalizacji zawału – zawał przedniej ściany serca przebiega na ogół ciężej niż zawał dolnej jego ściany. Celem leczenia jest przywrócenie przepływu przez zamkniętą tętnicę wieńcową aby zminimalizować uszkodzenie mięśnia sercowego. Już w karetce choremu podawany jest tlen, nitrogliceryna, leki przeciwpłytkowe i działająca przeciwbólowo morfina. Podawane są również beta-blokery, przeciwkrzepliwa heparyna, zmniejszające ciśnienie inhibitory ACE i w razie konieczności leki uspokajające. Po pierwszym postępowaniu rozpoczyna się leczenie reperfuzyjne. W zależności od potrzeby polega ono na leczeniu fibrynolitycznym za pomocą leków lub leczenia inwazyjnego. Metody inwazyjne są preferowane ponieważ dają lepsze wyniki. Wykonuje się je za pomocą następujących zabiegów: przezskórne interwencje wieńcowe (PCI) – zaliczamy do nich angioplastykę wieńcową, aterektomię, brachyterapię, pomostowanie aortalno-wieńcowe (CABG)[8].
Powikłania
[edytuj | edytuj kod]Ocenia się, że 7–12% pacjentów z zawałem serca umiera w trakcie hospitalizacji (w związku z rozwojem metod leczenia liczby te zmniejszają się). Spośród tych pacjentów, którzy opuszczają szpital, w ciągu pierwszego roku umiera 5–15% pacjentów. Te same dane statystyczne dotyczą też osób, u których dochodzi do ponownego zawału w roku następnym[1].
Wczesne
[edytuj | edytuj kod]Do nich zalicza się[38]:
- zgon, najczęściej w wyniku nagłego zatrzymania krążenia w mechanizmie migotania komór
- wstrząs kardiogenny - leczenie farmakologiczne i/lub kontrpulsacją aortalną[39]
- poszerzenie się ogniska zawałowego (najczęściej w wyniku poszerzenia się obszaru uszkodzenia reperfuzyjnego lub wstecznego narastania zakrzepicy w zajętej tętnicy wieńcowej)
- zaburzenia rytmu serca i przewodnictwa - leczenie farmakologiczne i/lub czasowa elektrostymulacja serca z użyciem nieinwazyjnych przezskórnych kardiostymulatorów[40]
- ostra niewydolność serca z obrzękiem płuc - leczenie farmakologiczne i/lub kontrpulsacją aortalną[39]
- ostra dyskineza mięśnia sercowego (ostry tętniak serca) - leczenie kardiochirurgiczne[41]
- pęknięcie ściany serca (tamponada serca) lub przegrody międzykomorowej (pozawałowy ubytek w przegrodzie międzykomorowej) - inwazyjne leczenie kardiologiczne lub kardiochirurgiczne[42]
- pęknięcie mięśnia brodawkowatego i ostra niewydolność zastawki mitralnej - inwazyjne leczenie kardiologiczne lub kardiochirurgiczne[43]
Ocena ostrej niewydolności serca
[edytuj | edytuj kod]Do oceny ostrej niewydolności serca związanej ze świeżym zawałem mięśnia sercowego, stosowana jest czterostopniowa klasyfikacja Killipa-Kimballa[22].
| Stopień | Charakterystyka | Fizykalnie |
| I | brak cech niewydolności serca | bez cech zastoju w krążeniu płucnym, brak III tonu serca |
| II | niewydolność serca | zastój w krążeniu płucnym, osłuchowo wilgotne rzężenia nad polami płucnymi poniżej dolnych kątów łopatek, obecny III ton serca |
| III | obrzęk płuc | zastój w krążeniu płucnym, osłuchowo wilgotne rzężenia nad polami płucnymi sięgające powyżej połowy wysokości płuc |
| IV | wstrząs kardiogenny | hipotonia, hipoperfuzja obwodowa, często łącznie z obrzękiem płuc, spadek skurczowego ciśnienia krwi poniżej 90 mm Hg |
Późne
[edytuj | edytuj kod]Do nich zalicza się[38]:
- zakrzepica przyścienna w komorze nad obszarem zawału i inne powikłania zatorowo-zakrzepowe
- pozawałowe zapalenie nasierdzia (łac. pericarditis epistenocardiaca) - leczenie farmakologiczne
- przewlekły tętniak serca - leczenie farmakologiczne i/lub kardiochirurgiczne[41]
- przewlekła niewydolność krążenia - leczenie farmakologiczne i/lub terapia resynchronizująca[44]
- zespół ramię-ręka - leczenie farmakologiczne
- zespół pozawałowy Dresslera - zalecane niesteroidowe leki przeciwzapalne, np. ibuprofen (leki z grupy steroidów nie są zalecane z powodu tendencji zmniejszania grubości i wytrzymałości blizny pozawałowej serca, która może prowadzić do jej pęknięcia)[45]
Rehabilitacja
[edytuj | edytuj kod]Rehabilitację rozpoczyna się po ustąpieniu bólu zawałowego, zmniejszeniu aktywności enzymów i obniżeniu temperatury jeszcze podczas pobytu pacjenta w szpitalu[46][47].
Faza I
[edytuj | edytuj kod]- Model A – stosuje się dla chorych z pełnościennym, niepowikłanym zawałem.
- 1° – ćwiczenia bierne i sadzanie po 2-3 dobach
- 2° – ćwiczenia czynne i pionizacja po 4-5 dobach
- 3° – wolne spacery oraz chodzenie po schodach po ok. 6–10 dniach
- Model B – dla chorych z powikłanym zawałem i trwa powyżej 21 dni.
W pierwszej fazie obciążenie nie powinno przekraczać 1,5-3 METów.
Faza I zazwyczaj kończy się wypisaniem chorego ze szpitala[46][47].
W pierwszym okresie zawału bardzo istotne jest zapewnienie lekkostrawnej diety, tak aby chory nie miał trudności z wypróżnianiem się. Defekacja jest dość dużym wysiłkiem, wymagającym napięcia tłoczni brzusznej, powodując odruchową tachykardię w celu zwiększenia rzutu sercowego. Skutkiem tego wysiłku może być „śmierć na sedesie” – dość typowa u chorych w pierwszych dwóch tygodniach choroby, czasami nawet z pęknięciem ściany serca.
Faza II
[edytuj | edytuj kod]Rehabilitacja może być kontynuowana w domu lub w jednym z wyspecjalizowanych ośrodków zamkniętych lub półotwartych: w sanatoriach kardiologicznych, oddziałach rehabilitacji kardiologicznej oraz poradniach rehabilitacji kardiologicznej zapewniających ciągły monitoring chorego, posiadających ruchome bieżnie lub cykloergometry. Wszystkie te zabiegi odbywają się pod nadzorem lekarza i rehabilitantów. Program ćwiczeń fizycznych tworzony jest na podstawie prób wysiłkowych na cykloergometrze (rower stacjonarny) lub bieżni mechanicznej. Pod uwagę bierze się także wyniki badań kardiologicznych – m.in. badań echokardiograficznych serca, monitoringu tętniczego krwi i ultrasonografii dopplerowskiej. Proste ćwiczenia chory powinien wykonywać w domu. Drugi etap rehabilitacji trwa od 4 do 12 tygodni[46][47].
Faza III
[edytuj | edytuj kod]Późna rehabilitacja kardiologiczna opiera się przede wszystkim na wprowadzeniu zmian do dotychczasowego trybu życia, aby utrzymać organizm w dobrej kondycji i zminimalizować ryzyko nawrotu schorzeń. Konieczna jest dalsza okresowa kontrola lekarza rodzinnego i kardiologa. Ten etap rehabilitacji trwa przez całe życie[46][47].
Telemetria w rehabilitacji
[edytuj | edytuj kod]Bardzo dobre efekty daje rehabilitacja z wykorzystaniem nowoczesnych narzędzi telemetrycznych – tzn. chory wykonuje ćwiczenia w domu podłączony do aparatu (holter + urządzenie telekomunikacyjne: modem, radio, komórka) pod kontrolą zdalną ośrodka. Pozwala to dokładniej monitorować pacjenta i znacząco obniża koszty rehabilitacji. Niestety w chwili obecnej NFZ nie refunduje jeszcze takich procedur medycznych[47].
Historia rozpoznania zawału mięśnia sercowego
[edytuj | edytuj kod]W 1876 roku Adam Hammer (1818 - 1878) zdiagnozował jako pierwszy zawał serca spowodowany zamknięciem tętnicy wieńcowej u żyjącego pacjenta, który następnie został potwierdzony pośmiertnie podczas sekcji zwłok[48].
W latach 90. XIX w. Ludvig Hektoen zauważył, że zawał serca jest skutkiem zakrzepu w tętnicy wieńcowej, a zmiana ta jest wtórna do zmian miażdżycowych, co opublikował w 1892 roku w periodyku medycznym[49].
W pionierskich badaniach zaznaczył się polski uczony Edward Sas Korczyński — 15 stycznia 1887 roku opublikował w krakowskim Przeglądzie Lekarskim, organie Towarzystw Lekarskich Krakowskiego i Galicyjskiego, pracę pod tytułem „Zator tętnicy wieńcowej serca za życia rozpoznany”[50].
W 1910 rosyjscy lekarze Wasilij Parmenowicz Obrazcow i Nikołaj Dymitriewicz Strażesko jako pierwsi opisali pod względem klinicznym pięć przypadków zawału serca, które potwierdzono następnie podczas autopsji[51]. Jednoznaczny związek przyczynowy pomiędzy zakrzepicą tętnic wieńcowych a zawałem serca ustalił amerykański lekarz James Bryan Herrick w 1912 roku[52].
Klasyfikacja ICD10
[edytuj | edytuj kod]| kod ICD10 | nazwa choroby |
|---|---|
| ICD-10: I21 | Ostry zawał mięśnia sercowego |
| ICD-10: I21.0 | Ostry zawał serca pełnościenny ściany przedniej |
| ICD-10: I21.1 | Ostry zawał serca pełnościenny ściany dolnej |
| ICD-10: I21.2 | Ostry zawał serca pełnościenny o innej lokalizacji |
| ICD-10: I21.3 | Ostry zawał serca pełnościenny o nieokreślonym umiejscowieniu |
| ICD-10: I21.4 | Ostry zawał serca podwsierdziowy |
| ICD-10: I21.9 | Ostry zawał serca, nieokreślony |
| ICD-10: I22 | Ponowny zawał serca |
| ICD-10: I22.0 | Ponowny zawał serca ściany przedniej |
| ICD-10: I22.1 | Ponowny ostry zawał serca ściany dolnej |
| ICD-10: I22.8 | Ponowny ostry zawał serca o innej lokalizacji |
| ICD-10: I22.9 | Ponowny ostry zawał serca o nieokreślonym umiejscowieniu |
| ICD-10: I23 | Niektóre powikłania występujące w czasie ostrego zawału mięśnia sercowego |
| ICD-10: I23.0 | Krwiak osierdzia jako powikłanie występujące w czasie ostrego zawału serca |
| ICD-10: I23.1 | Ubytek przegrody międzyprzedsionkowej jako powikłanie występujące w czasie ostrego zawału serca |
| ICD-10: I23.2 | Ubytek przegrody międzykomorowej jako powikłanie występujące w czasie ostrego zawału serca |
| ICD-10: I23.3 | Pęknięcie ściany serca bez krwiaka osierdzia jako powikłanie występujące w czasie ostrego zawału serca |
| ICD-10: I23.4 | Pęknięcie strun ścięgnistych jako powikłanie występujące w czasie ostrego zawału serca |
| ICD-10: I23.5 | Pęknięcie mięśnia brodawkowatego jako powikłanie występujące w czasie ostrego zawału serca |
| ICD-10: I23.6 | Skrzeplina w przedsionku, uszku przedsionka i komorze jako powikłanie występujące w czasie ostrego zawału serca |
| ICD-10: I23.8 | Inne powikłania występujące w czasie ostrego zawału mięśnia sercowego |
Zobacz też
[edytuj | edytuj kod]Przypisy
[edytuj | edytuj kod]- ↑ a b c d e f g h i j k l m n o p q r s t Therapie des akutem Herzinfarktes bei Patienten mit ST-Streckenhebung (STEMI) (Version 2017). leitlinien.dgk.org. [dostęp 2025-09-08]. (niem.).
- ↑ Causes of death in the EU – Statistics in focus 10/2006
- ↑ a b c d e f Grant W Reed, Jeffrey E Rossi, Prof Christopher P Cannon: Acute myocardial infarction. The Lancet, 2017, Volume 389, Issue 10065, P197-210. www.thelancet.com. [dostęp 2025-09-09]. (ang.).
- ↑ a b c d e f g Jacek Jąkała: Ocena metodą ultrasonografii wewnątrznaczyniowej i wirtualnej histologii wyników przezskórnych interwencji wieńcowych u pacjentów z zawałem serca. s:7012. dl.cm-uj.krakow.pl:8080. [dostęp 2025-09-15]. (pol.).
- ↑ a b Kristian Thygesen, Joseph S. Alpert, Harvey D. White. Universal Definition of Myocardial Infarction. „Circulation”. 116, s. 2634–2653, 2007. DOI: 10.1161/CIRCULATIONAHA.107.187397. [dostęp 2018-06-12]. (ang.).
- ↑ a b c Kristian Thygesen, Joseph S. Alpert, Allan S. Jaffe, Maarten L. Simoons, Bernard R. Chaitman, Harvey D. White. Third Universal Definition of Myocardial Infarction. „Circulation”. 126 (16), s. 2020–2035, 2012. DOI: 10.1161/CIR.0b013e31826e1058. [dostęp 2018-06-12]. (ang.).
- ↑ a b c d e f Program zabiegowego leczenia ostrego zawału serca. www.ikard.pl. [dostęp 2025-09-08]. (pol.).
- ↑ a b c d e f g h i Zawał serca – objawy, pierwsza pomoc, diagnostyka, leczenie. zdrowie.pzu.pl. [dostęp 2025-09-09]. (pol.).
- ↑ a b c d e f g ZAWAŁ SERCA - Patofizjologia I Mechanizm. leksykon.com.pl. [dostęp 2025-09-16]. (pol.).
- ↑ Abed Janoudi, Fadi E. Shamoun, Jagadeesh K. Kalavakunta, George S. Abela: Cholesterol crystal induced arterial inflammation and destabilization of atherosclerotic plaque. European Heart Journal, Volume 37, Issue 25, 1 July 2016, Pages 1959–1967. academic.oup.com. [dostęp 2025-09-09]. (ang.).
- ↑ ZATOR TĘTNICY WIEŃCOWEJ. leksykon.com.pl. [dostęp 2025-09-16]. (pol.).
- ↑ a b Prinzmetal M, Kennamer R, Merliss R, Wada T, Bor N. Angina pectoris. I. A variant form of angina pectoris; preliminary report. „Am J Med”. 27, s. 375–88, 1960. PMID: 14434946.
- ↑ Andrzej Szczeklik (red.) - Choroby wewnętrzne. Przyczyny, rozpoznanie i leczenie, tom I. Kraków: Wydawnictwo Medycyna Praktyczna, 2005, s. 149–150, język polski, ISBN 83-7430-031-0
- ↑ a b c ZAWAŁ SERCA PIERWSZA POMOC – JAK SZYBKO GO ROZPOZNAĆ?. pcrm.com.pl. [dostęp 2025-09-08]. (pol.).
- ↑ Nicholas G. Kounis. Kounis syndrome: an update on epidemiology, pathogenesis, diagnosis and therapeutic management. „Clin Chem Lab Med. (CCLM)”. 54, 10, s. 1545–1559, 2016. DOI: 10.1515/cclm-2016-0010. PMID: 26966931.
- ↑ Dotan Algranati 1, Ghassan S Kassab 2, Yoram Lanir. Why is the subendocardium more vulnerable to ischemia? A new paradigm. „Am J Physiol Heart Circ Physiol.”. 300 (3), s. 1090–1100, 2010. DOI: 10.1152/ajpheart.00473.2010. PMID: 21169398.
- ↑ a b c d Buja LM: Myocardial ischemia and reperfusion injury. Cardiovascular Pathology (2005), 14, 4, pp. 170-175. ournals.lww.com. [dostęp 2025-09-16]. (ang.).
- ↑ Ewa Podolecka: Czy można zmniejszyć uszkodzenie reperfuzyjne w ostrym zawale serca? (artykuł poglądowy). Artykuł poglądowy/Review article Kardiologia Polska 2010; 68, 12: 1385–1390 | access date 2025.09.15, language: pl
- ↑ a b c Ćwiczenie 1. PATOMORFOLOGIA UKŁADU KRĄŻENIA. a.umed.pl. [dostęp 2025-09-15]. (pol.).
- ↑ a b c Sekcja anatompatologiczna Sekcja anatompatologiczna zwłok ludzkich. www.umw.edu.pl. [dostęp 2025-09-15]. (pol.).
- ↑ Jak boli ręka przy zawale? Sprawdź, która ręka drętwieje? [online] [dostęp 2022-01-02] (pol.).
- ↑ a b c d e f g h i j k OSTRY ZAWAŁ SERCA. www.wl.cm.umk.pl. [dostęp 2025-09-08]. (pol.).
- ↑ a b c d e f g ZAWAŁ SERCA - Diagnostyka I Diagnoza. leksykon.com.pl. [dostęp 2025-09-16]. (pol.).
- ↑ A. Kirchgatterer - DIE KARDIALEN TROPONINE: WIRD DIE BEDEUTUNG ÜBERSCHÄTZT?. www.kup.at. [dostęp 2025-09-09]. (niem.).
- ↑ [https://web.archive.org/web/20120607202028/http://www.mdausa.org/publications/quest/q71ss-cktest.html Simply Stated . . . The Creatine Kinase Test]. web.archive.org. [dostęp 2025-09-09]. (ang.).
- ↑ a b Łukasz Figiel, Małgorzata Wraga, Zbigniew Bednarkiewicz at all - Direct comparison of the diagnostic value of point-of-care tests detecting heart-type fatty acid binding protein or glycogen phosphorylase isoenzyme BB in patients with acute coronary syndromes with persistent ST-segment elevation. www.kup.at. [dostęp 2025-09-09]. (niem.).
- ↑ NEW BLOOD TEST QUICKLY DETECTS EARLIEST SIGNS OF HEART ATTACK. hub.jhu.edu. [dostęp 2025-09-17]. (ang.).
- ↑ Med-Mythen: Warum steigt bei Krebs die LDH?. www.doccheck.com. [dostęp 2025-09-09]. (niem.).
- ↑ Heart attack [online], nhs.uk, 24 października 2017 [dostęp 2023-05-29] (ang.).
- ↑ Aspirin for heart attack: Chew or swallow? [online], Harvard Health, 1 maja 2005 [dostęp 2023-05-29] (ang.).
- ↑ a b c d [https://journals.viamedica.pl/choroby_serca_i_naczyn/article/view/54829/42405 Jarosław Gorol, Lech Poloński: Droga do nowoczesnego leczenia zawału serca — jakie były początki, gdzie jesteśmy obecnie? Choroby Serca i Naczyń Tom 14, Nr 4 (2017) (Opublikowany online: 2017-12-06)]. web.archive.org. [dostęp 2025-09-11]. (ang.).
- ↑ J. Mark Peterman, Anil George, Gregory R. Giugliano, Marc J. Schweiger, Door-to-Balloon Time, „Journal of the American College of Cardiology”, 56 (2), s. 158–159, DOI: 10.1016/j.jacc.2010.01.058 [dostęp 2018-01-24].
- ↑ a b Religa 1993 ↓, s. 247-268.
- ↑ Oldroyd KG. Complete Immediate Revascularization of the Patient With ST-Segment-Elevation Myocardial Infarction Is the New Standard of Care. „Circulation”. 135 (17), s. 1571–1573, 2017 Apr 25. DOI: 10.1161/CIRCULATIONAHA.117.025265. [dostęp 2017-04-26]. (ang.).
- ↑ MARIUSZ GĄSIOR LECH POLOŃSKI - Zawał mięśnia sercowego w Polsce – gdzie byliśmy, gdzie jesteśmy, dokąd zmierzamy?. publikacje.pan.pl. [dostęp 2025-09-17]. (pol.).
- ↑ Zalecenia ESH/ESC dotyczące leczenia nadciśnienia tętniczego – 2007 rok, Polskie Towarzystwo Kardiologiczne, Nadciśnienie tętnicze – nowe standardy ESC.
- ↑ A.Prejbisz, A.Januszewicz, Miejsce inhibitorów konwertazy angiotensyny w leczeniu nadciśnienia tętniczego i chorób współistniejących, Choroby Serca i Naczyń 2012, tom 9, nr 4, 208–213.
- ↑ a b DIAGNOSTYKA POWIKŁAŃ ZAWAŁU SERCA. klinikapoznan.pl. [dostęp 2025-09-08]. (pol.).
- ↑ a b Intra-aortic balloon pumping. web.archive.org. [dostęp 2025-09-09]. (ang.).
- ↑ Gacek A., Gałecka J., Prochaczek F., Kargul W., Wojciechowski D.: Elektrostymulacja oraz defibrylacja elektryczna serca, s:16-19. studylibpl.com. [dostęp 2025-09-09]. (pol.).
- ↑ a b Religa 1993 ↓, s. 269-280.
- ↑ Religa 1993 ↓, s. 281-285.
- ↑ [https://www.ahajournals.org/doi/pdf/10.1161/CIR.0000000000000029 Rick A. Nishimura, Catherine M. Otto, Robert O. Bonow at all.: 2014 AHA/ACC Guideline for the Management of Patients With Valvular Heart Disease: Executive Summary A Report of the American College of Cardiology/American Heart Association Task Force on Practice Guidelines]. www.ahajournals.org. [dostęp 2025-09-09]. (ang.).
- ↑ Resynchronisationstherapie gegen Herzschwäche. herzstiftung.de. [dostęp 2025-09-09]. (niem.).
- ↑ Yehuda Adler, Philippe Charron, Massimo Imazio at all.: 2015 ESC Guidelines for the diagnosis and management of pericardial diseases. pmc.ncbi.nlm.nih.gov. [dostęp 2025-09-09]. (ang.).
- ↑ a b c d Rehabilitacja kardiologiczna po zawale – ile trwa i jak wygląda?. sportsmedic.pl. [dostęp 2025-09-08]. (pol.).
- ↑ a b c d e Oddział Rehabilitacji Kardiologicznej. wim.mil.pl. [dostęp 2025-09-08]. (pol.).
- ↑ Adam Hammer (1818 - 1878) - Anmerkungen zu einem vergessenen Pionier der Ätheranwendung in der Geburtshilfe.. www.thieme-connect.com. [dostęp 2025-09-17]. (niem.).
- ↑ LUDVIG HEKTOEN: EMBOLISM OF THE LEFT CORONARY ARTERY; SUDDEN DEATH. Med Newsl (Lond). 1892; 61: 210–210.. pmc.ncbi.nlm.nih.gov. [dostęp 2025-09-16]. (ang.).
- ↑ Korczyński ES. Zator tętnicy wieńcowej za życia rozpoznany. Przegl Lek. 1887; 3. | language: pl
- ↑ Obrastzow WP, Straschesko ND. Zur Kenntnis der Thrombose der Koronararterien des Herzens. Z Klin Med 1910;71:116-32. | language: de
- ↑ [https://jamanetwork.com/journals/jama/article-abstract/433082 JAMES B. HERRICK: CLINICAL FEATURES OF SUDDEN OBSTRUCTION OF THE CORONARY ARTERIES. JAMA Published Online: December 7, 1912 1912;LIX;(23):2015-2022. doi:10.1001/jama.1912.04270120001001]. jamanetwork.com. [dostęp 2025-09-16]. (ang.).
Bibliografia
[edytuj | edytuj kod]- Piotr Gajewski. Uniwersalna definicja zawału serca. „Medycyna Praktyczna”. 1 (203) styczeń, s. 47–64, 2008. ISSN 0867-499X.
- Ostre zespoły wieńcowe, praca zbiorowa pod red. Grzegorza Opolskiego, Krzysztofa Filipiaka i Lecha Polońskiego. Elsevier Urban & Partner, Wrocław, 2002, ISBN 83-87944-43-2.
- Peter Mathes, Poradnik zawałowca, Włodzimierz J Musiał (tłum.), Warszawa: Wyd. Lekarskie PZWL, 1996, ISBN 83-200-1971-0, OCLC 835223190.
- Zawał serca: diagnostyka, leczenie, rehabilitacja, Zbigniew Nowak; Skrypt AWF, Katowice, 2003, ISBN 83-87478-64-4.
- Nowa strategia leczenia zawału serca (zasady organizacji małopolskiego programu interwencyjnego leczenia zawału serca) Dariusz Dudek, Krzysztof Żmudka; Krakowskie Wydawnictwo Medyczne, Kraków 2002, ISBN 83-88614-08-8.
- Serce i Ty, prof. Andrzej Kaliciński, Wyd. Medyk, Warszawa 1999, ISBN 83-87340-31-6.
- Co radzi lekarz. Choroby serca, red. Bernard Gersh, Wyd. Świat Książki, Warszawa 2006, ISBN 978-83-7391-862-7.
- Choroby serca i naczyń 2012, tom 9, nr 4, 208-213, Aleksander Prejbisz, Andrzej Januszewicz: Miejsce inhibitorów konwertazy angiotensyny w leczeniu nadciśnienia tętniczego i chorób współistniejących.
- Zbigniew Religa, Zarys kardiochirurgii, wyd. I, Warszawa: Wydawnictwo Lekarskie PZWL, 1993, ISBN 83-200-1732-7.
Linki zewnętrzne
[edytuj | edytuj kod]- Zawał serca – podstawowe informacje (pol.)
- Wytyczne ESC dotyczące postępowania w ostrym zawale serca. ptkardio.pl. [zarchiwizowane z tego adresu (2013-08-01)]. (pol.).
- Film instruktażowy – pierwsza pomoc przy zawale serca (pol.)
- Co (dalej) po zawale? – Program edukacyjny Polskiego Towarzystwa Kardiologicznego (pol.)










